アボガドロの法則
イタリアの科学者アボガドロ(1776-1856)は、気体との間の反応を説明するために、分子概念を導入しました。彼の理論によると、同じ温度と圧力でのすべての気体の体積は、分子の数に比例します。
すなわち、気体の種類に関係なく、同じ温度と圧力で同じ体積の気体中に含まれている分子の数は同じです。
アボガドロの分子説
アボガドロは、原子模型では、気体の反応の体積比が整数比で成立することを説明できないことを知っていました。これを解決するために、分子の概念を最初に提案しました。水素と酸素が反応して水蒸気が生成される反応を分子モデルとして表すと、次のとおりです。
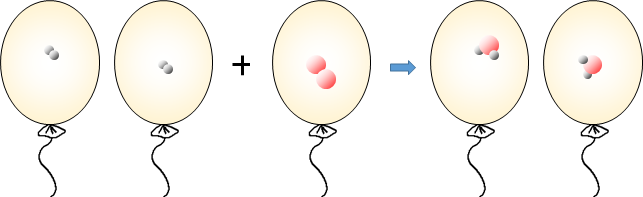
このように、分子モデルとして気体の反応を示すと、反応の前後に原子の種類と数が変わらず、気体の体積との間に一定の整数比成立し、原子が割れもありません。したがって、分子モデルは気体が反応したときに成立する体積比をうまく説明することができます。これらの説明に基づいてアボガドロは、気体が原子に存在するのではなく、原子が集まって成り立った分子として存在すると考えました。これが、分子概念の誕生です。分子モデルから分かるように、分子は原子が結合してなる粒子であり、物質の性質を帯びた最も小さな粒子です。